Строение металлов. Часть 3.
В зависимости от условий опыта и металла окисные пленки на нем могут быть получены различной толщины. В таблице 1 приведены толщины различных окисных пленок.
Таблица 1.
Толщина окисных пленок на некоторых металлах

Рост защитных пленок, а, следовательно их толщина, быстро увеличивается по мере повышения температуры. Так, уже при температуре 400° С на железе или обычной стали появляются видимые пленки окислов толщиной 720 Å. При температуре до 600° С поверхность покрывается довольно толстым слоем окалины. Такого рода пленка обладает еще некоторыми защитными свойствами. Повышение температуры выше 600° С приведет к дальнейшему росту пленки и ослаблению ее защитных свойств.
Окалина, образующаяся на железе, имеет сложное строение. Она состоит из слоев различных окислов железа, начиная от закиси и кончая окисью. На рисунке 11 дана схема строения окалины на железе. Из всех окисных слоев наибольшими защитными свойствами обладает непосредственно прилегающая к железу закись железа; другие слон, состоящие из окислов железа, не обладают этими свойствами, так как они пористы, содержат множество трещин и не препятствуют проникновению кислорода и влаги воздуха к металлу.

Рис. 11. Строение окалины на железе.
Таким образом, при соприкосновении поверхности металла с атмосферой, в которой содержится кислород, даже в случае полного отсутствия влаги в атмосфере, на поверхности металла возникают пленки, появление которых и есть один из видов коррозии. Эти пленки у разных металлов и условия их образования неодинаковы.
Всегда ли пленки защищают металл?
Из повседневной жизни мы знаем, что большинство металлических изделий (фермы, мосты, станки, сельскохозяйственные орудия), а также некоторые предметы домашнего обихода (швейные машины, телефонный аппарат, перочинный нож. ножницы, дверные ручки и т. д.) несут свою службу на воздухе, т. е. не соприкасаются с растворами электролитов. Наблюдения показывают, поверхность металлических изделий, даже не защищенная покрытием, в атмосферных условиях может время не изменяться.
Почему это происходят? Это происходит потому что на поверхности создается пленка из окислов, придающая, как говорят, пассивность металлам.
Особенно хорошо пленки защищают металлы, которые легко окисляются кислородом воздуха. К ним, в частности, относится алюминий. Почему же алюминий, имеющий большое сходство к кислороду, не корродирует? Дело в том, что окисная пленка из алюминия отличие от окисных пленок на других металлах сплошная и непроницаемая. Пленку нельзя увидеть простым глазом. так как ее толщина составляет всего 0,00001 см. Вес её с площади в 1 м2 не более 0,02 г.
Эта пленка как бы одевает поверхность металла непроницаемой одеждой, защищает от внешней среды. А что будет, если с алюминия снять эту одежду? Проделаем такой простой опыт. Натрем поверхность алюминия ртутью или раствором соли ртути. Ртуть растворяет окисную пленку и, следовательно, будет препятствовать ее образованию. При этом алюминии будет быстро окисляться (корродировать). На его поверхности появятся игольчатые кристаллы окислов, как показано на рис. 12. Алюминий, лишенный защитного слоя, энергично реагирует и с водой.
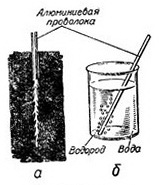
Рис. 12. Коррозия алюминия.
А можно ли искусственно получить прочную коррозионно устойчивую пленку? Возьмем для этой цели две стальные пластинки или два обычных гвоздя. Тщательно очистим их наждачной бумагой, сполоснем холодной водой. Один из образцов (пластинку или гвоздь) осторожно поместим в концентрированную азотную кислоту на 1 — 2 мин. Этого достаточно для образования на поверхности образца защитной (пассивной) пленки. — образец промоем для удаления остатков азотной кислоты. Опустим запассивированный и незапассивированный образцы в разбавленный (10—20%) раствор серной кислоты (рис. 13). Незапассивированный образен будет растворяться, что можно обнаружить по выделению пузырьков газа на его поверхности, в то время как запассивированные будет растворяться. Образовавшуюся защитную пленку на железе (образце) можно легко снять. Для этого достаточно к поверхности образца прикоснуться медной проволокой. Пленка «сползет», образуя на нижнем конце маленькую каплю. Если после этого опустить образец снова в слабый раствор серной кислоты, он будет растворяться, как незапассивнрованный.

Рис. 13. Пассивная железа азотной кислоты.
Образование прочных окисных пленок, которые удерживаются на поверхности металла и создают защитный слой, представляет пример «полезной коррозии», т. е. коррозии, которая задерживает дальнейшее разрушение. К такому виду защиты относят и азотирование стали. Азотирование стали в промышленных условиях проводят в атмосфере аммиака при температуре свыше 500 — 650° С. При этих условиях аммиак распадается на атомы водорода и азота. Атомы азота в момент своего образования являются очень активными и взаимодействуя с атомами железа, образуют нитриды железа. Прочная пленка нитридов железа, покрывающая поверхность защищает металл от вредного влияния кислорода, а также паров воды, находящихся в воздухе. Нужно сказать, что образующиеся нитриды металла не только защищают металл от дальнейшего разрушения, но и придают поверхностному слою металла повышенную твердость и прочность на истирание.
Очень часто в практике прибегают к образованию на поверхности металла пленок, получающихся в результате взаимодействия железа с углеродом. Это явление носит название науглероживания или цементации.
При цементации стальные изделия помещают в атмосферу окиси углерода при высокой температуре. При этом углерод соединяется с железом и получается так называемые карбиды железа, прочно покрывающие поверхность металла. Здесь мы опять встречаемся с полезной коррозией, которая защищает металл от дальнейшего разрушения.
Строение металлов. Часть 3.
Основные положения пленочной теории пассивного состояния металлов были высказаны английским ученым М. Фарадеем в 1836 г. Согласно взглядам Фарадея, пассивное состояние, т. е. такое состояние, когда металл не разрушается под влиянием внешней среды, объясняется тем. что поверхность металла покрывается слоем окисла металла и кислорода, предупреждающим дальнейшее его разрушение. Однако многие ученые возражали против теории пассивности металлов, потому что окисные пленки были невидимы и существование их было сомнительно. Только за последнее время при помощи тонких оптических методов было установлено наличие таких невидимых пленок на поверхности железа в пассивном состоянии. Толщина этих пленок достигала 40—100 Å. Условия возникновения тонких пленок, делающих металл пассивным, были изучены английским ученым Ю. Р. Эвансом и советским ученым В. А. Кистяковским. Пассивность металла, по его (Кистяковского) утверждению, вызывается образованием на поверхности металла тонкой, бесцветной стекловидной и неэлектропроводной пленки окисла, которая надежно защищает металл от воздействия внешней среды. Кистяковский показал, что пассивной пленкой на поверхности металла является не всякая, которая появляется в результате взаимодействия металла с кислородом, а только такая, которая появляется на поверхности, подвергшейся особой обработке, например, полировке.
Почему защитные пленки возникают только на поверхности, тщательно отшлифованной и отполированной, в то время как металл, грубо обработанный, не образует такого рода пассивной пленки? Оказалось, что при его обработке (шлифовке и полировке) кристаллы поверхностного слоя разрушаются, сжимаются и на поверхности образуется тонкий аморфный слой, т. е. слой с разрушенными кристаллами (рис. 14). Этот слой однороден и, более активно взаимодействуя с кислородом, образует стекловидную защитную пленку. В зависимости от условий возникновения строение и толщина пленки могут быть различными. Пленка может быть пористой. Через эти поры к металлу проникают вещества, которые вызывают дальнейшую его коррозию. Тогда пленка уже не играет защитной роли, а, наоборот, способствует развитию коррозии. Присутствие таких пленок на металле Кистяковский назвал активным состоянием поверхности металла, в отличие от пассивного состояния, когда пленка предохраняет металл от разрушения. В зависимости от условий возможен самопроизвольный переход от одного состояния поверхности металла к другому. Эта теория Кистяковского была подтверждена исследованиями как наших отечественных, так и зарубежных ученых.
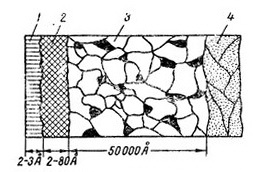
Рис. 14. Строение металла с шлифованной поверхностью.
В зависимости от условий образования пленок их можно разделить на группы:
1.Пленки не содержат пор, трещин и полностью изолируют металл от коррозионной среды. Такие пленки получают на поверхности стальных и железных изделий, тщательно отполированных и отшлифованных, а также таких хорошо окисляющихся металлов, как алюминий и цинк.
2.Пассивной может быть пленка, имеющая поры. Торможение процесса коррозии в этих случаях может происходить за счет сопротивления, которое оказывают поры протеканию электронов с анодных участков на катодные.
3.Наконец, могут образоваться толстые пленки, рыхлые, с трещинами, свободно пропускающими кислород воздуха к поверхности металла, а также другие газы и пары воды. Такие пленки не защищают металл от коррозии, а, наоборот, усиливают ее. Примером такой пленки может служить ржавчина.
Следовательно, не всякая пленка может защищать поверхность металла. Наряду с пленочной теорией пассивности металла имеется еще так называемая адсорбционная теория пассивности. Сущность адсорбционной теории сводится к тому, что пленки создают не на всех участках металла, а только на катодах и анодах и тем самым разрушают работу микрогальванических элементов на поверхности, делая ее пассивной.